目录
温馨提示:
本方案目录中的内容在word文档内均有详细阐述,如需查阅,请购买后下载。
说明
一、如招标文件要求“项目背景及需求分析”,详情见本方案的第一章;
二、如招标文件要求“项目整体服务设想”,详情见本方案的第二章;
三、如招标文件要求“项目组织机构及人员配备”,详情见本方案的第三章;
四、如招标文件要求“项目拟投入的设施设备”,详情见本方案的第四章;
五、如招标文件要求“项目管理规章制度”,详情见本方案的第五章;
六、如招标文件要求“艾滋病防治知识宣传服务方案”,详情见本方案的第六章;
七、如招标文件要求“服务质量保障方案”,详情见本方案的第七章;
八、如招标文件要求“档案管理方案”,详情见本方案的第八章;
九、如招标文件要求“应急预案”,详情见本方案的第九章。
编制依据
一、项目招标文件、补遗及设计文件等相关资料。
二、国家现行技术规范、标准及有关的技术资料、规范、规程及技术标准。
三、依照有关主要法律、法规:
(一)《中华人民共和国政府采购法》
(二)其他法律法规。
四、行业规范、标准
(以下内容根据招标文件及项目实际情况进行修改)
第一章 项目背景及需求分析
第一节 艾滋病背景分析
一、艾滋病的起源
(一)艾滋病的发现与命名
1981年6月,美国医疗控制中心出版的《病死率和发病率周报》(MMWR)报道了美国洛杉矶5例男性同性恋者患卡氏肺孢子虫肺炎。同年7月美国疾病预防与控制中心又发现在过去的两年半,共有26位男性同性恋者患罕见的卡波西肉瘤。这些疾病既往仅见于免疫缺陷的病人,且很少发生。这些病例预示着一种新的疾病开始流行。这些病人的共同特点是:
1.同性恋者。
同时根据病人的症状预示着可能是通过性传播的一种新的传染病。
2. 卡氏肺孢子虫肺炎。通常正常人是不会发生这种疾病的,只有在免疫力低下时,才会发生这种机会性感染。因此认为,这可能是由于免疫系统损坏(即免疫缺陷)后,由各种微生物或寄生虫引起的。
3. 常见卡波西肉瘤。这种疾病在黑种人青年中较常见,而在白种人青年中很少见,只在60岁以上老年人中发现。同时认为这种奇特的疾病可能是经过性传播得传染病,这种病原会破坏免疫系统形成免疫缺陷,并伴有机会性感染。1982年,将这种新的疾病命名为“获得性免疫缺陷综合征”(acquired immunodeficiency syndrome,AIDS),中文翻译成艾滋病。
这种严重致死性疾病的突然出现,立即引起国际医学界的高度重视,并开始探索这种新的传染病的病原和病因。这种新的疾病传播很快,在美国发现后很快在欧洲也被发现,很多科学家开始研究这种病的病因。1983年,法国巴斯德研究所肿瘤研究生主任Montagnier首次报道从1例患持续性全身淋巴腺肾病综合征的男性同性恋者取出重大的淋巴结组织,在体外进行细胞培养,经过培养他们在电镜下见到一种与反转录病毒相似的病毒。用实验室多种方法进行研究证明这是一种新的病毒,命名为“淋巴腺病相关病毒”(lymphaednopathy associated virus,LAV)。患这种病的病人有LAV抗体。
1984年,美国肿瘤研究中心Gallo等也报道从艾滋病病人的外周血淋巴细胞中分离出一种新病毒,命名为人类嗜T细胞病毒Ⅲ型(human T cell lymphotropic virus type Ⅲ,HTLV Ⅲ)。为什么Gallo称这种病毒为HTLV—Ⅲ呢?因为Gallo在1978年从蕈样真菌病病人的淋巴结建立了T白血病细胞株,发现其中有一种新的RNA反转录病毒,称为人T细胞白血病病毒(HTLV—Ⅰ),后来证明此病毒是在日本发现的成年人T细胞白血病的病因。不久Gallo又从毛细胞性白血病病人的细胞株分离到一株新病毒,命名为HTLV—Ⅱ,由于从艾滋病病人中分离到的病毒与HTLV—Ⅰ都是反转录病毒和嗜T细胞。因此,称这种病毒为HTLV—Ⅲ。稍后,美国加州大学旧金山分校Levy也从艾滋病病人外周血细胞分离到一种新病毒,命名为艾滋病相关病毒(AIDS related virus,ARV)。这3种病毒的形态、核酸序列、蛋白结构、细胞嗜性均相同,但各自命名不同。1986年6月,国际微生物学会及病毒分类学会统一将LAV、HTLV—Ⅲ、ARV这3种名称统一起来,称为人类免疫缺陷病毒(human immunodificiency virus,HIV)。
(二)艾滋病起源学说
1978年,从美国实验室储存的血清中查到艾滋病病毒抗体,但从1972~1973年在乌干达采集的血清中也可以查到艾滋病病毒抗体。从这些回顾性血清学调查的结果来看,艾滋病病毒感染人最初在非洲。
目前发现,艾滋病病毒有HIV—1和HIV—2两个型。文献报道,从猩猩中分离到3株猴免疫缺损病毒(SIV)cpz,它与HIV—1有关。他们是在加蓬捕捉的猩猩分离到2株SIVcpzGAB1和SIVcpzGAB2及从赞比亚进口到比利时的猩猩分离到的病毒SIVcpzANT。其中,SIVcpzGAB1和SIVcpzANT已经完成全核酸序列的分析。
美国Alabama大学的高峰等发现一只非洲进口的猩猩,应用酶联免疫吸附测定(ELISA)及蛋白印迹法(Western blot)检测,它的血清能与HIV—1抗原起很强的反应。此动物从未用过艾滋病病毒有关研究,也未接受过人工的血清。研究显示猩猩的祖先就有病毒重组,并与HIV—1有核酸序列杂交现象。因此,认为HIV—1来源于猩猩。
HIV—2与从非洲白眉猴分离的猴免疫缺陷病毒SIVsm和SIVmac近似。这种猴是SIV的储存宿主。HIV—2与HIVsm的基因序列的同源性为70%,而与HIV—1的同源性仅为40%左右。猴免疫缺陷病毒感染的猴血清能与HIV—2的糖蛋白(gp120和gp36)和壳蛋白的P24等发生免疫反应,但不与HIV—1的糖蛋白起反应。因此,认为HIV—2型来源于SIVsm。
以下证据认为HIV是从动物传到人的:
1.病毒的基因结构是相似的;
2.系统数相关;
3.在自然宿主中流行;
4.地理分布一致;
5.合理的传播途径。例如,在白眉猴中发现的SIVsm在遗传系统上与HIV—2很相似,而且其产地与HIV—2的流行区也一致。
从研究结果看出,HIV—1和HIV—2也与从猩猩和猴子来源的病毒很相似,而且这些动物可能就是HIV—1和HIV—2的储存宿主。当地人民生活习惯喜欢猎食猴子和猩猩为食物,或作为宠物饲养。这些动物与人接触密切,就将病毒传入人类,艾滋病首先发源于非洲,经人传至海地,海地首都太子港色情文化开放,是同性恋者的天堂,吸引了很多美国同性恋者到那里寻欢作乐。他们在那里感染了HIV,然后带回到美国。由于男性同性恋的性伴侣多,很容易将HIV传播,所以,在流行早期多是同性恋者患艾滋病,但不久后逐渐传播到静脉吸毒者和异性恋者。最后酿成美国的暴发流行,并逐渐扩散至全球。
艾滋病是人类历史上最具破坏性的疾病。自从类人猿将病原体传染给人类,HIV已经感染了7500万人。近年发表在《科学》杂志上的一项研究首次揭示了世界艾滋病大流行是何时、何地及怎么爆发与起源的。根据对HIV所有可用基因数据的统计分析,一个由牛津大学和比利时鲁汶大学领导的国际研究团队已经确认这个灾难爆发于1920年的金沙萨,现在的刚果民主共和国的首都。将这个结果与历史数据进行对比分析,研究人员解释了这个病毒如何从一个被感染的黑猩猩传染给人类。
根据病毒的基因组测序和最新的亲缘地理学技术,研究人员已经重建了疫情的遗传史。此前,科学家发现南喀麦隆的黑猩猩是艾滋病的源头。在整个艾滋病出现的历史上,有几个人被这些类人猿传染了,但这些病例中仅有1例导致了艾滋病在人类中的传播。
为了确定疫情起源的时间和地点,研究人员比较了在刚果盆地国家收集的病毒的遗传多样性,考察疫情潜在的发源地。结果是:这场灾难起源于金沙萨,现在的刚果民主共和国的首都,可以追溯到1920年。
一旦艾滋病病毒的地理起源地被确定,科学家能够将病毒进化的基因数据与历史数据进行比较,来确定病毒在金沙萨暴发和人类之间传播的情况。比利时殖民档案显示,20世纪初,在喀麦隆东南部和金沙萨之间的流域贸易繁荣(如象牙、橡胶等)。这可以解释为什么人类的疫情暴发在刚果首都而不是发现黑猩猩将疾病传染给人类的喀麦隆。
1920~1950年,随着城市化进程和交通的便利,特别是铁路的发展,使金沙萨成为中部非洲的枢纽。20世纪40年代末,每年有超过100万人通过金沙萨到达该国的北部或南部,或前往邻国。这些不寻常的混合因素,结合病毒的遗传适应性,导致病毒在全国的迅速蔓延及在非洲南部和东部的二次暴发。20世纪60年代之后,随着社会的变化,如性交易增多与公共健康措施方面未消毒注射针的使用,无疑造成了疫情从小规模暴发到真正的大流行。
二、艾滋病基本知识
(一)HIV感染及艾滋病定义
1.HIV感染
(1)HIV病毒
艾滋病的病原体为人类免疫缺陷病毒(human immunodeficiency virus,HIV),能够导致人类免疫系统的功能缺陷。HIV病毒于1983年在法国巴斯德研究所分离获得,1986年由国际微生物学会及病毒分类学会统一命名。它是一种单链RNA(ribonucleic acid,核糖核酸)病毒,属于反转录病毒科慢病毒属中的人类慢病毒组(lentivirus)。该病毒主要破坏人体的免疫功能,导致人体的免疫系统失去抵抗力,使得人体极易合并各种机会性感染、免疫缺陷性疾病和癌症等,最终导致死亡。
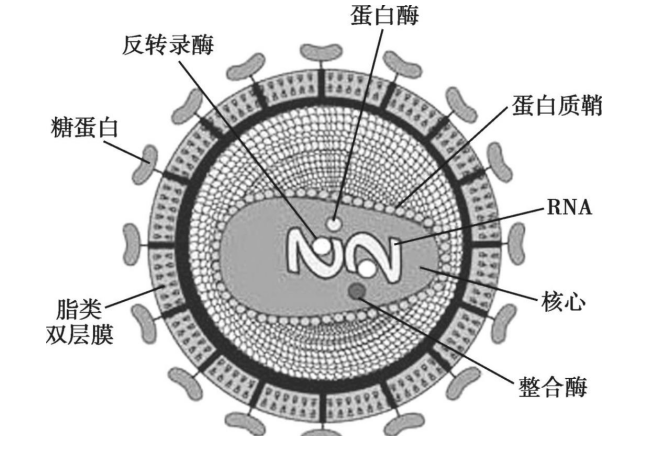
(2)病毒基本类型、基本形态与结构
根据HIV基因差异,划分为HIV—1型和HIV—2型。大多数的艾滋病是由HIV—1型引起,HIV—2型主要在西非流行。HIV病毒大致呈球形,病毒直径约120nm,基本结构如图1—1所示。病毒外膜是脂类双层膜,来自宿主细胞,并嵌有病毒的糖蛋白gp120与gp41;gp41是跨膜蛋白,gp120位于表面,并与gp41通过非共价作用结合。向内是由蛋白p17形成的球形基质(matrix),以及蛋白p24形成的半锥形衣壳(capsid),即蛋白质鞘。衣壳内含有病毒的RNA基因组、酶(反转录酶、整合酶、蛋白酶)以及其他来自宿主细胞的成分。
(3)HIV病毒对外界抵抗力
HIV在体外对外界理化和环境因素的抵抗力低。对热敏感,56℃、30分钟能使HIV在体外对人的T淋巴细胞失去感染性,但不能完全灭活血清中的HIV;100℃、20分钟可将HIV完全灭活。HIV能被75%乙醇、0.2%次氯酸钠及次氯酸钙灭活。紫外线和γ射线均不能灭活HIV。HIV侵入人体可刺激其产生抗体,但主要为非中和抗体,血清同时存在抗体和病毒时仍有传染性。
(4)HIV感染过程及机制
HIV入侵人体后,主要导致CD4+T淋巴细胞的破坏和功能丧失,继而使机体出现慢性进行性的免疫功能缺陷。CD4+T淋巴细胞也称“T辅助细胞”,主要作用是免疫应答,在免疫系统中承担信号传导作用,当这些细胞数量减少则直接导致免疫信号不能传递、机体免疫力下降。健康成人CD4+T淋巴细胞每微升全血中的数量为800~1200个,HIV感染者CD4+T淋巴细胞数量与体内病毒载量、感染程度及时间有关,普遍表现为低于健康成人的CD4+T淋巴细胞数量。当其CD4+T淋巴细胞数量低于100个/mm3时,表明患者机体抵抗力极其低下,极易发生机会性感染和发生肿瘤,表现出明显的艾滋病相关临床症状和体征。
HIV进入机体后,感染巨噬细胞、树突状细胞和其他黏膜组织中CD4受体的细胞,刺激机体细胞免疫系统活化,出现临床急性感染。此时,病毒大量复制,病毒复制大约持续2个月,因此,很容易在患者血液和淋巴液中分离到病毒。在感染早期或初期,大量的病毒颗粒迅速播散到机体的各个器官,尤其是淋巴结、脾脏、扁桃体和腺状体。在暴露2~4周后,70%以上的HIV感染者出现流感样的症状,临床表现为全身酸痛、乏力、发热、皮疹、夜间盗汗等症状,在临床上容易被误诊为流感。另一部分人则没有任何不适感觉。此时,患者体内的免疫系统中的杀伤T细胞(CD8+T细胞)和B细胞产生的抗体发挥作用,病毒免疫应答产生后,抗体与病毒发生中和反应,病毒的滴度迅速下降,大部分病毒被清除,但也有一部分病毒没有被清除,而是进入了宿主细胞。从感染发生到可检测到抗体称之为“窗口期”。所谓“窗口期”(window period)是指感染者从感染病毒到可以检测到特异性抗体的这段时间,由于个体间存在免疫应答差异,窗口期不是一个固定的天数,一般而言抗体检测的窗口期为4~12周。随着检测技术敏感性的提高,窗口期在不断缩短,抗原检测可将窗口期缩短至2~3周,核酸检测的窗口期最短,一般为5~10天。
此后HIV感染者进入长期携带病毒而无临床症状的潜伏期,潜伏期的病毒载量维持在低水平,但病毒的复制仍在继续。如果未经抗病毒治疗,潜伏期一般可达8~10年,感染者在潜伏期内,可以不出现任何临床症状;约5%感染者的潜伏期可以到12年以上,其间CD4+T淋巴细胞数量仍然可以保持正常且无临床症状。经历8~10年的潜伏期后患者进入艾滋病期,患者会出现各种艾滋病临床表现、症状或体征。然而,也有10%的HIV感染者可在感染的2~3年内迅速发展成为HIV患者(快速进展者),或反之,病程进展十分缓慢(长期存活者)。造成这种差异的原因与患者个体的年龄、遗传、毒株的毒力以及其他病原微生物合并感染的影响有密切关联。
尽管HIV感染者常没有明显的临床表现,但是病毒却从来没有停止复制。当大量毒力强的病毒株出现后,导致机体内出现第二次高滴度的病毒血症。同时CD4+T淋巴细胞数量降低到200个/mm3以下,机体免疫系统出现损伤,感染者就会出现多种临床体征。
2.艾滋病
(1)艾滋病定义
艾滋病全称为获得性免疫缺陷综合征(AIDS),是由HIV感染引起的以获得性细胞免疫功能缺陷为特征。临床表现为淋巴结肿大、慢性腹泻、体重减轻、发热等全身性疾病,进而发展出现各种机会性感染、肿瘤、神经系统疾病等多种症状,最终导致死亡的传染病。
(2)艾滋病与HIV感染关系
HIV侵袭人体免疫系统,破坏人体对感染的自然防御,从而导致免疫系统功能逐渐低下,最后衰竭。艾滋病是HIV破坏机体免疫功能后出现的一系列病理综合征,临床表现多样化,主要为多病原体的复合感染。迸发各种机会性感染或肿瘤是导致艾滋病患者死亡的主要原因。
随着病毒对感染者免疫系统的进一步损害,感染者在临床上将会出现更严重的体征。机会性感染就是艾滋病的主要病症和死因。机会性感染是指对正常人而言的条件性致病微生物,但对艾滋病患者而言可以引起感染和临床改变,并可能导致死亡。
(3)艾滋病诊断
当一个人经艾滋病初筛或快速诊断检测为阳性时,需进一步经蛋白印迹确证实验阳性做出感染HIV病毒的诊断。在我国部分高流行地区也可采取替代方法进行诊断。在确认阳性后,通常采用对其CD4+T淋巴细胞监测判断其疾病进展。在临床上如HIV感染者出现机会性感染或肿瘤,也可据此诊断其已发展为艾滋病期。当某人被诊断为艾滋病患者后,并不代表其会很快死亡,尤其是现在通过服用抗病毒药物,可以控制和改善其临床症状,从而延长寿命。
(4)艾滋病的主要临床表现、症状及体征
进入艾滋病期的患者因为细胞免疫系统受到严重的破坏,机体免疫力下降,容易发生各种机会性感染和恶性肿瘤。艾滋病患者症状没有特异性,表现为复杂多样的综合征。常见症状包括长期低热,短期内体重减轻十分之一以上、消瘦、乏力、盗汗、慢性腹泻、咳嗽、全身淋巴结肿大、头晕、头痛、智力减退、反应迟钝等。患者出现机会性感染,或者肿瘤、侵犯器官或系统而出现相关的症状和体征,如侵犯呼吸系统则出现咳嗽甚至呼吸困难等呼吸系统的症状和体征,侵犯消化系统则出现慢性腹泻等症状。HIV患者常见的肿瘤主要以卡波西肉瘤最为多见,多侵犯皮肤或者肺部。皮肤出现深蓝色或紫色的斑丘疹或结节。除了卡波西肉瘤以外,其他肿瘤如淋巴瘤、肝癌、肾癌等也多常见。
(二)HIV传播途径
HIV的传播几率主要与机体接触到的病毒数量、毒力以及病毒进入机体的途径有关。在人体血液、精液、阴道分泌物、母乳、深部体液如脑脊液、胸腹腔积液、羊水等均可分离到病毒。因此,可以确定HIV传播途径与这些体液的存在形式和人们接触这些体液的行为有关。HIV的传播途径主要有性传播、血液传播和母婴传播。
1.性接触途径传播
性接触传播是目前我国HIV的主要传播方式与流行的高危险因素。艾滋病是重要的性传播疾病(sexually transmitted diseases,STDs)之一。在北美洲、欧洲和澳大利亚等国家中,以在男同性恋人群中传播为主;而在非洲、东南亚、部分南美洲和加勒比海等国家中,则以在异性恋者中传播为主。接触血液、精液和阴道分泌液均有可能感染。在精液中人类免疫缺陷病毒的浓度高于阴道分泌物,因而从理论上支持传播从男性到女性比女性到男性更容易的假设。
HIV感染人体后,可将其基因组整合到人体细胞内,因而感染者将终身携带病毒,同时成为终身传染源。感染个体性伙伴的血清阳转率差异非常显著,在血友病HIV感染者的性伴侣中阳转率为10%~20%,而在艾滋病患者的性伴侣中阳转率可达20%~75%,说明与患者体内的病毒浓度(病毒载量)有关。除此之外,HIV在不同个体的传染性是不一样的,也与性接触的方式和次数有一定的关系。但仅这一点并不能解释如此大的差异。有的个体仅一次不安全的性接触就感染了HIV,但另一些个体在数百次不安全的性接触后仍未被感染HIV。所以这些差异也与个体的抵抗力、不同的病毒株、感染个体传染性的变化、增强或减弱传染性的辅助因子等有关。
在男男性接触者(men who have sex with men,MSM)人群中,HIV传播最危险的因素是接受肛门性交和具有多个男性性伙伴。肛门性交的危险性明显高于仅有口交的个体感染风险。接受肛交的女性具有更大的危险性。坚持使用安全套可避免HIV的传播。
2.经血途径传播
HIV可通过输血、血液制品、注射等方式传播。
(1)输血或者输血液制品传播
如果血液里有HIV,输入此血者将会被感染。输注HIV污染的血液制品也可传播HIV。有些患者(例如血友病)需要注射由血液中提取的某些成分制成的生物制品,如果灭活不彻底,这些血液制品中有可能有HIV,使用这些血液制品就有可能感染上HIV。
(2)污染针具传播
使用不洁针具可以把HIV从一个人传到另一个人。静脉吸毒者共用注射器或注射器消毒不彻底是感染HIV的危险因素。医疗场所使用污染的针具、输液器等也可造成HIV经血传播。
(3)医源性感染
主要是指医疗器械(具)不洁或消毒不彻底(如透析、有创诊疗和拔牙工具)等,造成接受医疗服务者感染HIV。医源性传播也包括医护人员在提供医疗服务时,暴露于感染者/患者的体液而导致感染HIV。不慎被污染HIV的器具如针头刺伤皮肤,或黏膜直接接触到含有HIV的体液也可能导致感染。被污染的锐器刺伤单次暴露的传染概率为0.3%~0.5%。
3.母婴途径传播
母婴传播指的是HIV阳性的妇女可通过宫内、产程和产后母乳喂养等将HIV传染给新生儿,是儿童感染HIV的主要途径。HIV的传播主要发生在三个时期:产前、产时和产后。
(1)产前感染
也就是宫内感染,即HIV通过胎盘感染胎儿。HIV可越过胎盘的绒毛膜屏障,引起宫内感染。
(2)产时传播感染
这是母婴传播最主要的途径,即分娩时胎儿通过母亲的产道,接触含有HIV表面抗原的血液或体液等,引起感染。胎儿在产时如果发生皮损后接触母血及羊水也可感染HIV。
(3)产后感染
是指产后采取母乳喂养时,新生儿可能通过吸食HIV阳性母亲的母乳存在感染HIV的风险(详见第六章第二节)。
4.其他
如接受HIV感染者的器官移植、人工授精或污染的器械等可感染HIV。科学证据表明HIV不会通过食物、水、昆虫传播,也不会通过握手、拥抱、礼节性亲吻、同吃同饮、共用厕所和浴室、办公用具、公共交通工具、娱乐设施等日常生活接触传播。
(三)HIV感染机制
HIV主要侵犯人体免疫系统,包括CD4+T淋巴细胞、巨噬细胞和树突状细胞,主要表现为CD4+T淋巴细胞数量不断减少,导致并发严重机会性感染和肿瘤等。
1.病毒动力学
HIV进入人体后,24~48小时内到达局部淋巴结,5天左右在外周血中可以检测到病毒成分。继而产生病毒血症,导致以CD4+T淋巴细胞数量短期内一过性迅速减少为特征的急性感染。大多数感染者未经特殊治疗,CD4+T淋巴细胞可自行恢复至正常或接近正常水平。但病毒并未被消除,形成慢性感染。慢性感染包括无症状感染期和有症状感染期。无症状感染期时间可达数年不等。
2.HIV感染与复制
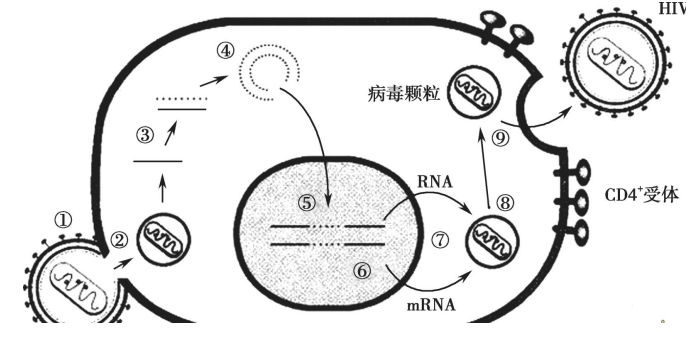
(①吸附;②脱衣壳;③反转录;④环化;⑤整合;⑥转录;⑦翻译;⑧核心颗粒组装;⑨HIV的组装和出芽;)
HIV需借助易感细胞表面的受体进入细胞,HIV—1的gp120首先与第一受体-CD4细胞结合,然后与第二受体-嗜淋巴细胞受体(CXCR4)和趋化因子受体(CCR5)结合,根据HIV与第二受体结合的特征,HIV可分为R5和X4毒株。R5毒株只有利用CCR5受体,而X4毒株可同时利用CCR5、CXCR4和CCR3受体。HIV和受体结合后,gp120构想改变与gp41分离,与宿主细胞膜融合进入细胞。在反转录酶作用下HIV RNA链反转录成负链脱氧核糖核酸(deoxyribonucleic acid,DNA)。在胞核内DNA聚合酶(DNA polymerase,DNAP)作用下复制成双联DNA。后者部分存留于胞质,部分作为前病毒(provirus)。新形成的双链DNA整合于宿主染色体。潜伏2~10年后,前病毒可被激活,转录和翻译成新HIV RNA和病毒蛋白质,在细胞膜组装成新HIV后芽生释出,如图1—2所示。HIV感染宿主免疫细胞后以每天产生109~1010颗粒的速度繁殖,并直接使CD4+T淋巴细胞溶解破坏。病毒复制产生的中间产物及gp120、vpr等可诱导细胞凋亡。芽生释出后可感染并破坏其他细胞。
3.CD4+T淋巴细胞数量减少和功能障碍
(1)HIV对受感染细胞溶解破坏和诱导细胞凋亡直接损伤;gp120与未感染HIV的CD4+T淋巴细胞结合成靶细胞被CD8+细胞毒性T细胞(cytotoxic T cell,CTL)介导的细胞毒作用及抗体依赖性细胞毒作用(antibody—dependent cell—mediated cytotoxicity,ADCC)攻击而造成免疫损伤破坏,致CD4+T淋巴细胞减少;HIV可感染骨髓干细胞,使CD4+T淋巴细胞产生减少。
(2)CD4+T淋巴细胞的极化群Th1/Th2失衡:Th2呈极化优势,而抗病毒免疫应答弱化,抗原呈递功能受损、白介素(interleukin,IL)—2产生减少和对抗原反应活化能力丧失,使HIV/AIDS易发生各种感染。
2. 单核—吞噬细胞(mononuclear phagocyte,MP)功能异常
MP表面也有CD4分子,也可被HIV感染。吞噬细胞有对抗HIV感染所致细胞病变作用,但部分MP功能异常,抗HIV和其他病原体感染能力下降。HIV感染后,诱导产生一种与NF—κB核因子抗原性相结合因子,防止细胞凋亡,使HIV在MP中持续复制而成为病毒储存场所,并可携带HIV透过血脑脊液屏障,引起中枢神经系统感染。
5.B细胞功能异常
B淋巴细胞表面低水平CD4分子表达,可被HIV感染。感染HIV的B细胞功能异常,出现多克隆化,循环免疫复合物和外周血B淋巴细胞增高,对新抗原刺激反应降低等。
6.自然杀伤细胞(natural killer cell,NK细胞)异常
HIV感染者早期即有NK细胞数量减少。可因细胞因子产生障碍或HIV通过gp41直接抑制NK细胞的监视功能,使HIV感染者易出现肿瘤细胞。
7.异常免疫激活
HIV感染后,免疫系统可出现异常激活CD4+T淋巴细胞、CD8+T淋巴细胞表达CD69、CD38和HLA—DR等免疫激活标志物水平的异常升高,且与HIV血浆病毒载量有良好的相关性,随着疾病的进展,细胞激活水平也不断升高。
(一)HIV感染相关临床实验室检测
1. HIV—1/2抗体检测
(1)筛查试验
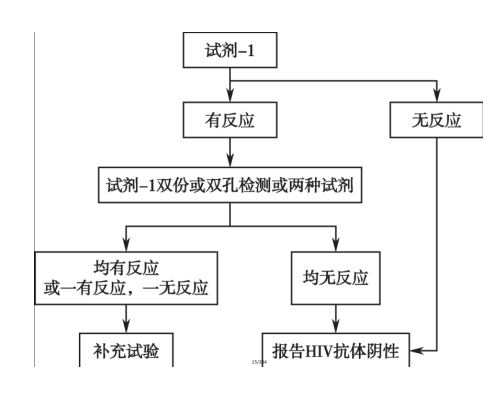
1)酶联免疫吸附试验(enzyme—linked immunosorbent assay,ELISA)是目前最常用的HIV抗体筛查试验。用于HIV抗体检测的ELISA试剂的发展已经历了四代,前两代是间接法试剂,现已趋于淘汰。第三代ELISA试剂方法学为双抗原夹心法,所用抗原为高度纯化的基因重组抗原或人工合成多肽(包括O群抗原),可同时检测IgG、IgM抗体,已成为我国目前在临床和血液筛查中使用的主要方法。第四代试剂可同时测定HIV—1/2抗体和p24抗原,称HIV抗原/抗体试剂。ELISA法检测HIV抗体的敏感性和特异性都超过99%。其假阴性结果通常出现在HIV感染最初的1~2周内或是疾病后期抗体水平很低的时候;而假阳性结果则可能与以下疾病相关:自身免疫性疾病、肾衰、胆囊纤维化、肝病、血液透析、多次妊娠或输血以及接种疫苗等。这类试验可使用血液(包含血清、血浆和滤纸干血斑)、尿液样本进行检测。对在筛查试验中无反应的样本,可报告为HIV抗体阴性,对有反应的样本,用原有试剂和另外一种不同原理(或不同厂家)的筛查试剂进行复检,复检均无反应的样本报告HIV抗体阴性,复检均有反应或一种筛查有反应、另一种无反应的样本,开展补充试验。HIV抗体筛查试验流程如图所示。
2)化学发光或免疫荧光试验:这类试验采用发光或荧光底物,可使用血液(包含血清和血浆)、尿液样品,既可检测抗体,也可联合检测抗原抗体。HIV抗原/抗体包被于固相载体,加入待检样品和酶或荧光标记的HIV抗原/抗体,加发光或荧光底物,用发光或荧光仪测定结果。有效试验的阴性和阳性对照必须符合试剂盒规定。
3)快速检测(rapid test,RT)及其他试验:这类试验可使用血液、口腔黏膜渗出液作为样本,操作简便快速,适用于应急检测、门诊急诊检测、预防母婴传播和自愿咨询检测门诊或VCT(HIV voluntary counseling and testing)及检测点等。一般可在10~30分钟内得出结果。实验操作人员需要经过培训方可操作此方法。
4)明胶颗粒凝集试验(gelatin particle agglutination test,PA):是HIV血清抗体检测的一种简便方法。其原理为将纯化的HIV抗原连接到红色明胶颗粒上制成致敏颗粒,当加入的检测标本中含有HIV抗体时,即可发生肉眼可见的凝集反应,根据凝集情况判读结果。PA方法操作简便,适合于小型实验室的HIV日常筛查工作,也可与ELISA方法配合用于筛查阳性标本的复检试验。
5)免疫渗滤试验:阳性结果在膜上抗原部位显示出有色斑点或条带。反应时间在10分钟以内。有效试验的质控点必须显色。
6)免疫层析试验:有效试验的质控带必须显色。反应时间在30分钟以内。
(2)补充试验
补充试验是通过检测样本中是否存在HIV抗体、抗原或者核酸而确定HIV感染的检测方法。补充试验包括抗体确证试验[免疫印迹试验(western blot,WB),条带/线性免疫试验(recombinant immunoblot assay/line immuno assay,RIBA/LIA),特定条件下的替代检测,免疫层析或免疫渗滤试验]和核酸检测试验(核酸定性检测和核酸定量检测试验)。替代检测包括三种酶联免疫试验、三种快速试验或酶联免疫加快速试验1。确证实验的目的是排除筛查的假阳性、进行流行病学调查、疫情报告及确定临床诊断。确证实验包括:放射免疫沉淀试验(radioimmunoprecipitation test,RIT)、免疫印迹法(western blot,WB)等。WB方法是目前公认的HIV抗体确证方法。以下对WB方法做一重点介绍。
特定条件:高流行地区(流行率大于5%)、高危人群(如男男同性恋、吸毒人群)、三种试剂均经过使用地区中心实验室评价。
1)WB法:
原理是以病毒抗原、重组抗原或合成肽,经SDS—PAGE电泳后转至硝酸纤维素膜上,再与血清或血浆中的HIV抗体结合,最后以显色反应来确定条带的存在。WB的敏感性一般不低于初筛实验,但它的特异性很高,这主要是基于HIV不同抗原组分的分离以及浓缩和纯化,能够检测针对不同抗原成分的抗体,因而能够用WB方法鉴别初筛实验的准确性。
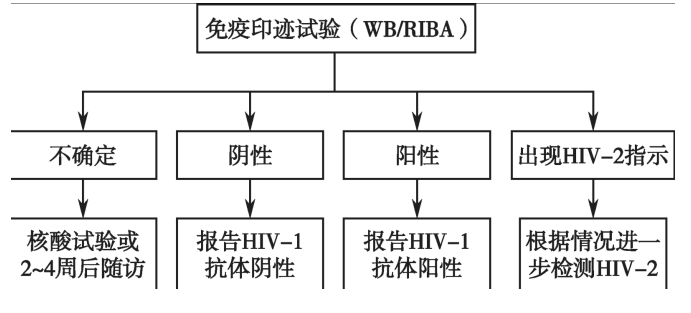
2)确证实验流程及结果报告:
有HIV—1/2混合型和单一的HIV—1或HIV—2型。先用HIV—1/2混合型试剂进行检测,如果呈阴性反应,则报告HIV抗体阴性;如果HIV—1条带呈阳性反应,则报告HIV—1抗体阳性;如果不满足阳性标准,则判为HIV抗体检测结果不确定。如果出现HIV—2型的特异性指示条带,需用HIV—2型免疫印迹试剂再做HIV—2的抗体确证实验。呈阴性反应,报告HIV—2抗体阴性;呈阳性反应则报告HIV—2抗体血清学阳性。符合HIV抗体不确定判断标准,报告“HIV抗体不确定(±)”,在备注中应注明等待“4周后复检”。
2. HIV病毒学检测
(1)p24抗原检测
机体感染HIV后,p24抗原是最早能从血清中检出的病原学标志,一般在HIV感染后2~3周就可以检测到,1~2个月可以达到高峰。随着HIV抗体的产生形成抗原/抗体复合物,因抗体的中和作用,p24的浓度下降至无法测出,标志着HIV感染者进入无症状期。当p24抗原再度在血液中增加,提示感染者即将或已经进入艾滋病期。因此,检测p24抗原主要是作为HIV抗体检测窗口期的辅助诊断,对于HIV感染窗口期或HIV阳性母亲所生婴儿的鉴别诊断有重要作用,同时也可以作为检测病程进展和判断预后的标准,对于评价药物及疫苗的抗病毒治疗效果也有一定的意义。
(2)病毒载量(viral load,VL)检测
用来测量人体外周血液HIV病毒含量。HIV病毒载量检测主要用于评估HIV感染的进程、确定抗病毒治疗方案、监测抗病毒治疗效果以及HIV感染早期的辅助诊断。HIV病毒载量检测的对象是HIV核糖核酸(HIV RNA),常用的检测方法有反转录—多聚酶链式反应(reverse transcription PCR,RT—PCR)、核酸序列依赖性扩增试验(nucleic acid sequence—based amplification,NASBA)和分支DNA扩增试验(branched DNA signal amplification assay,bDNA assay)等。主要的临床意义如下:
1)婴儿的早期诊断:
HIV感染母亲所生小于18个月龄的婴儿,不同时间的两次HIV核酸检测均为阳性即可做出诊断。18个月龄以上儿童诊断与成人相同:有急性HIV感染综合征或流行病学史,且不同时间的两次HIV核酸检测结果均为阳性,即可诊断。
2)病程监控及预测:
HIV感染发生后病毒载量变化具有一定规律,这种变化与疾病的进程有着密切的相关性。因此定期进行病毒载量检测有助于确定疾病发展的阶段,以确定相应的治疗方案。
HIV病毒载量与6年发病率的关系为:病毒载量<500拷贝/毫升时发病率为5.4%;501~3000拷贝/毫升时为16.6%,3001~10 000拷贝/毫升时为31.7%;10 001~30 000拷贝/毫升时为55.2%;>30 000拷贝/毫升时则为80%。当HIV感染者CD4+T细胞计数<200个/mm3时,病毒载量与3~6个月发展至AIDS的危险为:病毒载量<10 000拷贝/毫升时发病率为4.9%;10 000~29 999拷贝/毫升时为12.7%;30 000~99 990拷贝/毫升时为17.7%;>100 000拷贝/毫升时为22.4%。
3)指导抗病毒治疗及疗效判定:
通常在病毒载量达到一定水平后(如>35 000~50 000拷贝/毫升)抗病毒治疗才显示良好的治疗效果。治疗后,通过病毒水平的检测能够确定治疗是否有效。通常在治疗6个月后病毒水平降低0.5log以上才被认为临床有效。
4)耐药性监测:
可用于HIV耐药检测和监测,指导公共卫生医生了解耐药性病毒株流行的态势和指导临床医生判断抗病毒治疗效果和修改抗病毒治疗方案。
3.免疫状态检测
CD4+T淋巴细胞计数是衡量人体免疫功能的重要指标。HIV感染人体后侵犯CD4+T淋巴细胞,而出现CD4+T淋巴细胞进行性减少,CD4+T/CD8+T淋巴细胞比值倒置,细胞免疫功能受损。常用的淋巴细胞计数检测方法为自动检测方法,包括流式细胞仪(多平台法或单平台法)和专门的细胞计数仪。
正常人的CD4+T淋巴细胞计数约占总T淋巴细胞的65%,CD8+T淋巴细胞计数约占35%。人体CD4+T淋巴细胞计数值因种族、生活条件、生存环境不同而有所差别,如据报道湖北省健康成人CD4+T淋巴细胞计数均值为681个/mm3,上海地区成人CD4+T淋巴细胞正常平均值为726个/mm3。HIV感染人体后,随着CD4+T淋巴细胞数量的减少,机体免疫力下降,发生机会性感染的几率增加。临床上将CD4+T淋巴细胞计数<200个/mm3作为患者进入艾滋病期的参考指标之一。
准确可靠的CD4+T淋巴细胞检测是评价HIV感染者免疫状况、预测判断疾病进程、评价抗病毒药物治疗效果和估测预后的重要指标。监测HIV感染者及患者CD4+T淋巴细胞亚群计数值,分析其变化规律,对于评价免疫系统损害程度、准确判断疾病进程、延长感染者及患者的生存时间有重要的意义。
4.HIV耐药基因检测
HIV耐药性检测常用方法有基因型检测法和表型检测法。基因检查法原理是利用基因测序技术获得序列信息,系统判断是否耐药以及耐药的程度,其优势在于周期短、操作简便、重复性好,且花费较少。表型检测法包括传统的共培养方法和重组病毒检测方法,能直接测出HIV对药物的敏感度,并能揭示事先存在或交叉的耐药情况,有利于指导HIV感染者有效用药。耐药性检测主要用于HIV感染人群和抗病毒治疗人群的耐药性监测和检测,指导临床决策。
(五)HIV感染后疾病发展过程
HIV感染可分为急性HIV感染、无症状HIV感染和艾滋病期三期,其中急性HIV感染期、无症状HIV感染期的患者统称为HIV感染者,艾滋病期的患者称为艾滋病患者。不是每个感染者都会完整地出现三期表现。但每个疾病阶段的患者在临床上都可以见到。HIV感染人体后疾病的发展进程与身体内病毒载量、感染者体内的免疫状态密切相关,三者之间的关系见图。
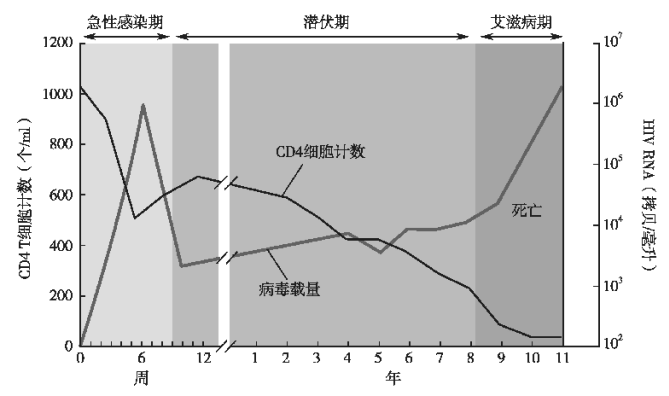
1.HIV感染临床表现与分期
(1)急性HIV感染的临床表现
艾滋病HIV感染通常表现为无任何症状,但也可表现为急性感染综合征,感染HIV到急性发病一般存在6天至6周的潜伏期,所以患者通常无法准确判断感染的时间。
急性HIV感染综合征通常表现为传染性单核细胞增多症样疾病,也有少量患者表现为急性神经性疾病及其他不同类型的综合表现。急性HIV感染综合征发病急,约有70%的患者在感染HIV后2~4周出现类似伤风、流感样的症状,表现为发热、寒战、全身乏力、食欲减退、关节疼痛、肌肉疼痛、全身淋巴结肿大等。在急性期阶段,常可查到P24抗原血症,随着HIV抗体的生成,形成抗原抗体复合物,抗原浓度将不断下降。
急性HIV感染综合征的患者中,大部分会出现全身淋巴结肿大。以颈后、颌下、腋下淋巴结肿大多见。肿大的淋巴结不融合,质硬,偶有压痛,表面皮肤无改变。
大约有75%的患者出现咽炎,表现为咽部充血、渗出及腭颊部溃疡。在其他的报道中也有病例表现为食管炎、食管溃疡等。
许多艾滋病患者是以皮肤损伤为首发症状,临床上多表现为皮疹、全身瘙痒、尖锐湿疣、接触性湿疣、荨麻疹等。有1/3~1/2的患者出现红色丘疹暴发。皮疹最早可出现于胸部和躯干,然后逐渐扩散到四肢。
另外,HIV具有嗜神经性,在急性感染中可表现为神经组织病变。患者可能出现急性非细菌性脑膜炎、非特异性白质变性等,表现为头痛、疲倦、神经性症状和脑膜刺激征,后期可发展成为严重痴呆。
在急性感染期,大多数症状会在2~3周后逐渐消失,但是淋巴结肿大、脾大、发热以及肌肉肿痛会持续数月。
(2)无症状HIV感染的临床表现
在急性期之后,患者的临床症状逐渐消失,但体内仍存在HIV,这一期间称为无症状HIV感染期,又称潜伏期。艾滋病潜伏期随着患者的年龄、感染途径、感染病毒的剂量及种类不同而有差别。据相关研究报道,目前普遍认为成年人潜伏期为8~10年。此外,也有少量患者经过急性期之后一直为持续性无症状状态。初次感染HIV的剂量较大,如输血感染,则潜伏期的持续时间将相对较短,儿童约1.9年,成人8.2年,老年人5.5年。通过性接触感染HIV的患者潜伏期时间一般较长,最长可达15年。
在潜伏期中,艾滋病患者常没有任何临床症状(但可有全身淋巴结肿大),但是并不代表此时艾滋病患者处于安全期。在此期间,患者体内的HIV仍在不断地大量复制,持续破坏人体免疫系统。
(3)艾滋病期的临床表现
经过无症状HIV感染期,艾滋病患者会逐渐出现一些与艾滋病相关的症状和体征,直至发展成为典型的艾滋病。此时为感染HIV后疾病进展的最终阶段,患者因免疫系统严重缺陷,出现艾滋病的各种指征性疾病,包括严重HIV消耗综合征、严重的机会性感染、HIV相关性肿瘤和中枢神经系统病变等病症。
方案完整版请点击:艾滋病防治宣传服务投标方案
觅模网是一家专门提供各行各业的投标资料模板,包括投标书、投标方案、技术方案、投标文件、商务标、标书模板/施工组织设计等内容,每一种行业都有多种投标资料模板,包括投标书中的商务标和技术标,还有各中行业资料。觅模网专业提供各种行业投标资料模板,找投标资料模板就上觅模网。

